Microbiota normal de la leche humana
Entre las bacterias que se encuentran de forma fisiológica en la leche humana destacan los estafilococos, los estreptococos y las bacterias lácticas. La mastitis es una auténtica disbiosis de la microbiota normal de la glándula mamaria, con un espectacular aumento de la concentración del agente causal, muy por encima de los límites normales, y la desaparición del resto de las bacterias «fisiológicas» de la leche. Como referencia, la concentración bacteriana total en la leche fresca de una mujer sin mastitis suele ser inferior a 2.000 bacterias/mL. El Staphylococcus epidermidis suele encontrarse en la leche de prácticamente todas las mujeres, pero su concentración máxima no debería ser superior a 600-800/mL. El Staphylococcus aureus se encuentra en un porcentaje minoritario de mujeres asintomáticas (<20%) y, en tales casos, su concentración suele ser inferior a 300-400/mL. Los estreptococos se hallan ampliamente distribuidos con una concentración habitualmente inferior a 500/mL.
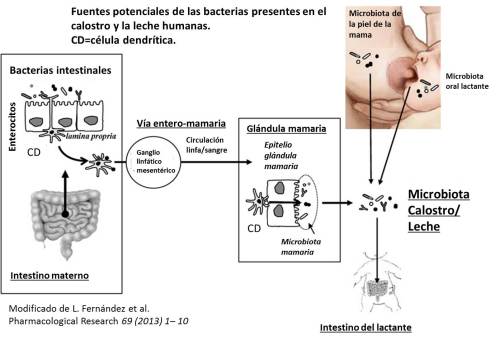
Cuando las mastitis se manifiestan por dolor intenso y síntomas inflamatorios (enrojecimiento, tumefacción, induración) y, con frecuencia, síntomas constitucionales como fiebre, malestar… las diagnostica cualquiera, son las mastitis agudas causadas el la mayoría de los casos, por Staphylococcus aureus cuya presencia en la glándula mamaria no es habitual. Cuando el tejido mamario reacciona tratando de aislar a las bacterias causantes de la mastitis en una cápsula de tejido conjuntivo, se produce un absceso.
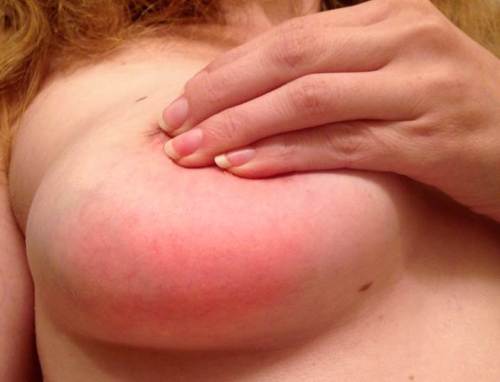
Mastitis aguda, probablemente por estafilococo aureus
Pero en la mayoría de los casos de mastitis clínica, sintomática, el único síntoma es un dolor intenso, acompañado ocasionalmente de síntomas locales, como grietas y/o zonas de induración, pero sin afectación sistémica. Estos casos no son los “de libro” pero son los más frecuentes y los que causan más destetes no deseados y, en consecuencia, merecen una atención especial. Se trata de las mastitis subagudas.
El dolor, más o menos intenso, típicamente en forma de “pinchazos” (referido en muchas ocasiones como “cristales”, “agujas”…, con calambres ocasionales (que pueden llegar a ser muy intensos y reflejarse en la espalda o el brazo) y, a veces, sensación de quemazón. El hecho de que no se suelan acompañar de enrojecimiento local ni de síntomas generales (como la fiebre) confunde frecuentemente el diagnóstico y provoca que se trate de un problema tan infravalorado como infradiagnosticado.
El dolor se debe a que las bacterias se disponen en forma de películas biológicas (biofilms) en el epitelio de los acinos y los conductos galactóforos. Si la concentración bacteriana rebasa los límites biológicos, la luz de los conductos se reduce, de manera que la presión que ejerce la leche sobre un epitelio que está inflamado es considerablemente mayor.

Representación esquemática del proceso de formación de una biopelícula o biofilm en el interior de los conductos galactóforos durante una mastitis.
Como consecuencia de ello, cuando se va acumulando la leche en los conductos o cuando se produce la eyección de ésta, se siente un dolor intenso en forma de «pinchazos».
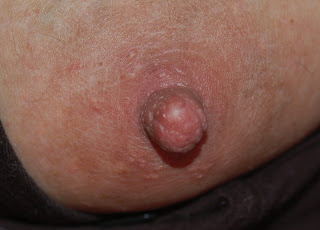
Perla de leche
En ocasiones, algunos de los conductos se pueden llegar a obturar completamente, lo que provoca una retención de leche que empeora los síntomas locales. Cuando estas obstrucciones ocurren en los propios orificios del pezón, se forman unas estructuras características, integradas por una matriz de calcio recubierta de bacterias, conocidas como “ampollas de leche” o “perlas de leche”.

Representación esquemática del epitelio y conductos mamarios en condiciones fisiológicas (A) y en situación de mastitis (B). Las flechas rojas indican el aumento de presión de la leche al pasar por una luz disminuida. esta presión sobre una zona inflamada es la responsable de los típicos “pinchazos”.
Las mastitis subagudas se deben a un sobrecrecimiento de ciertas especies de estafilococos coagulasa-negativos (Staphylococcus epidermidis), estreptococos de los grupos viridans/mitis (como Streptococcus mitis o Streptococcus salivarius) y algunas especies del género Corynebacterium. Todas ellas, a diferencia del Staphylococcus aureus, son habituales en la glándula mamaria durante la lactancia pero se detectan en concentraciones muy moderadas en la leche (<1.000 colonias/ml). De hecho, a tales concentraciones juegan un papel beneficioso para el niño sin suponer ningún problema para la madre, formando una película fina en las paredes internas de los conductos, permitiendo un flujo completamente normal de leche. La presión de la leche al salir hace que algunas de estas bacterias se pongan en suspensión en este fluido. Son, precisamente, las bacterias que se transfieren de la madre al hijo y las que se pueden detectar en un cultivo.

Mama de aspecto normal afectada por estafilococo epidermidis
Tanto las mastitis agudas como las subagudas suelen ir acompañadas de zonas de induración dentro del pecho y, en ocasiones, de grietas. Aunque las grietas se han asociado generalmente a la postura durante la toma o a la anquiloglosia (aspectos que se deben revisar ante dicho problema), no hay que descartar la implicación de las propias bacterias causantes de las mastitis en su etiopatogenia; en este sentido, los germenes causantes de estas mastitis son epidermiolíticas per se cuando se encuentran en concentraciones elevadas en las glándulas de Montgomery.
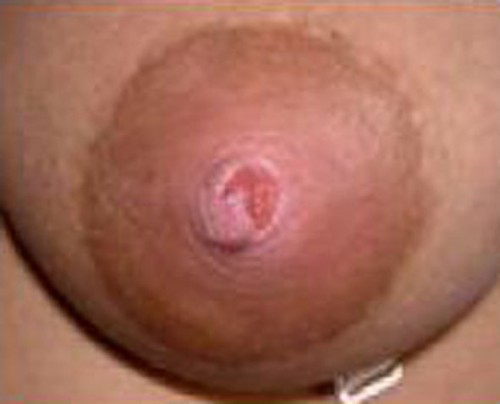
Grieta en el pezón asociada a mastitis estafilocócica
Diagnóstico diferencial del dolor en el pecho: (ver referencias 2. y 7. de la Bibliografía)
A toda mujer lactante que presente dolor en el pecho, acompañado o no de otros síntomas, se le debería recoger una muestra de leche lo antes posible para confirmar o descartar una mastitis infecciosa. La instauración sistemática de este tipo de análisis facilitaría un tratamiento más racional y eficaz. Además, ciertos signos pueden servir para descartar otros problemas que pueden cursar con dolor en el pecho/pezón. Cuando una mujer refiere dolor al amamantar, con o sin presencia de grietas, se suele valorar si la postura del niño al pecho es la correcta o si éste presenta algún tipo de problema (frenillo corto o anquiloglosia , micrognatia, macrognatia, reflejo hipertónico de lengua, etc.). Esta valoración se debe hacer lo más rápidamente posible y no debe sustituir, en ningún caso, a la toma de muestras para el análisis microbiológico. Hay muchos casos en que se pierde un tiempo precioso valorando la postura, cuando el problema real es una mastitis infecciosa. Los niños (incluidos los prematuros), al igual que las crías del resto de especies de mamíferos, manifiestan unos reflejos innatos, por lo que la frase «es que el niño no sabe mamar», escuchada demasiadas veces, está totalmente injustificada.
Otro problema que conviene descartar es el síndrome de Raynaud (SR), descrito originalmente como un vasospasmo de las arteriolas de las partes terminales del cuerpo, como los dedos de las manos y los pies, las orejas o la nariz. Este vasospasmo, a menudo provocado por el frío o por situaciones estresantes, causa una isquemia intermitente. Inicialmente, la parte afectada palidece hasta mostrar un aspecto marmóreo; posteriormente, cobra un color azul cianótico debido a la desoxigenación de la sangre venosa. Finalmente, se vuelve rojiza por la vasodilatación refleja. Además de este cambio trifásico (que también puede ser bifásico) en la coloración, se suelen presentar otros síntomas, como dolor intenso, sensación de quemazón y parestesia. En 1992, se sugirió que el vasospasmo que se produce en el pezón en ciertos casos de amamantamiento doloroso podría estar relacionado con el SR; posteriormente, se han descrito diversos casos. En la mayoría de ellos, la lactancia es el primer momento en que una mujer con SR manifiesta sintomatología, ya que los pechos están frecuentemente expuestos a la temperatura ambiental y sujetos a una estimulación mecánica. A pesar de ello, el SR es todavía bastante desconocido en los ámbitos ginecológico y pediátrico, teniendo en cuenta que estos profesionales pueden ser los primeros médicos en valorar a una paciente con este problema. Por tanto, no es raro que una mujer con SR sea tratada innecesariamente con antibióticos; de hecho, como el dolor no remite, suelen ser sometidas a sucesivos tratamientos con diversos agentes antimicrobianos. El análisis microbiológico de la leche permite identificar a mujeres con SR a quienes se había diagnosticado una mastitis infecciosa sobre la base del dolor. Además, hemos observado que un elevado porcentaje de mujeres con SR tienen antecedentes de problemas cardiovasculares. La sintomatología asociada a este problema se puede controlar con nifedipina, siguiendo un control médico.
Los síntomas y las lesiones asociadas a la mastitis tuberculosa mamaria (habitualmente en forma de nódulo irregular en los cuadrantes superior o central externos) pueden ser muy similares a las del carcinoma de mama. El diagnóstico diferencial se puede establecer mediante un análisis citológico, histológico y/o microbiológico.
Otra enfermedad rara que puede afectar al pecho es el herpes, y se suele desaconsejar la lactancia cuando las lesiones activas se localizan en el pezón. En este sentido, en nuestro laboratorio observamos que un caso de presunto herpes en el pezón se trataba realmente de una mastitis estafilocócica con infección e inflamación de las glándulas de Montgomery de la areola mamaria.
Mastitis subclínicas: se trata de cuadros causados generalmente por las mismas especies que las subagudas pero que no han alcanzado concentraciones que lleguen a superar el umbral del dolor. La etiopatogenia, el diagnóstico y el tratamiento son similares a los de las mastitis subagudas. Se caracterizan por una falsa sensación de poca producción de leche (que, en general, también sucede en los otros tipos de mastitis) y suelen corresponder con comentarios habituales del tipo “mi leche no alimenta al niño”, “no tengo suficiente leche”, “mi leche no es nutritiva”… En la gran mayoría de los casos ni la producción de leche está comprometida ni la composición nutricional es inadecuada; simplemente, la formación de densas biopelículas bacterianas en el interior de los conductos impide su correcta secreción.
La disminución del caudal de leche en las mastitis hace que las tomas sean más largas y/o frecuentes. El lactante pasa de estar tranquilo y relajado a estar irritable, tirando bruscamente del pezón y haciendo unos movimientos muy característicos con la cabeza. Para cualquier bebé (sobre todo en los más pequeños) la succión supone un esfuerzo físico importante. Las tomas prolongadas y el amamantamiento más agresivo favorecen que la glándula mamaria se siga inflamando determinando un círculo vicioso que empeora el problema.
No parece descabellado suponer que existe un continuidad entre la mastitis subclinica y la subaguda, es un problema de grado, de intensidad de la afectación. Esta mastitis silente podría ser muy frecuente y la responsable de la mayoría de las prescripciones de suplementos con sucedáneo por hipogalactia. En estos casos estaría indicado o bien el cultivo o bien el tratamiento empírico con lactobacillus (ver más adelante).
Mastitis granulomatosas : afortunadamente rara. Se trata de inflamaciones benignas de la glándula mamaria poco frecuentes pero cuyo diagnóstico suele crear confusión. Generalmente afectan a mujeres en edad fértil, algunos meses después de haber tenido un hijo. Habitualmente es un proceso unilateral que se manifiesta por una o más masas inflamatorias dolorosas, de consistencia firme y, a veces, con inflamación cutánea que casi siempre se ubica fuera de la areola mamaria y que pueden evolucionar hacia la formación de úlceras, abscesos, la fistulización y/o supuraciones crónicas. En este sentido, poseen un gran potencial para la deformación morfológica del pecho afectado. Al examinar las zonas inflamadas (bien externamente o bien mediante técnicas de imagen), estas se asemejan mucho a las que se observan en mujeres con carcinoma de mama. Por ello, inicialmente se suele sospechar de cáncer o, alternativamente, de tuberculosis.
Una vez que los análisis histopatológicos (imprescindibles para el diagnóstico diferencial) confirman que no se trata de ninguna de esas dos enfermedades, se suelen clasificar como mastitis granulomatosa, mastitis granulomatosa idiopática, mastitis lobular granulomatosa o lobulitis granulomatosa de “etiología incierta”. Histológicamente, las lesiones se caracterizan por una lobulitis crónica, necrotizante, no caseificante, con formación de granulomas. Los granulomas tienen una apariencia muy característica: una capa externa de histiocitos epitelioides que rodea a una colección de polimorfonucleares neutrófilos. A su vez, los polimorfonucleares neutrófilos se disponen alrededor de un espacio central aparentemente vacío, constituido por lípidos disueltos, motivo por el que también reciben el nombre de lipogranulomas supurativos.
Hasta hace apenas unos años, la etiología de estos procesos era desconocida. Actualmente, se sabe que la mayoría de estas estructuras están causadas por bacterias del género Corynebacterium. De hecho, el estudio más detallado de estos granulomas ha permitido observar la presencia de estas bacterias dentro de los espacios vacíos rodeados por los neutrófilos.
Corynebacterium kroppenstedtii es la principal causa de mastitis granulomatosas. Esta especie fue descrita, por primera vez, a partir de un aislado obtenido del esputo de una mujer con una infección respiratoria y se caracteriza por la ausencia de ácido micólico en su pared celular y la producción de una neuraminidasa que podría actuar como factor de virulencia. Se diferencia de otras corynebacterias por su carácter lipofílico, una propiedad que parece particularmente relevante en la patogenia de este tipo de mastitis. Su lipofilia le permite crecer firmemente adherida a los glóbulos de grasa y le proporciona acceso a una abundantísima fuente exógena de ácidos grasos. No es de extrañar que, en las preparaciones histológicas, esta especie se encuentre localizada en las vacuolas centrales que contienen lípidos. El hecho de que estas bacterias afecten especialmente a mujeres en edad fértil, entre algunos meses y pocos años después de haber tenido un hijo, sugiere que su sobrecrecimiento puede estar estrechamente ligado a la gran disponibilidad de ácidos grasos durante la lactancia. Dado que los granulomas se desarrollan lentamente es perfectamente posible que el cuadro aparezca incluso meses después de que haya finalizado la lactancia.
El mito de las cándidas: Muchos pediatras, matronas y asociaciones de lactancia creen, injustificadamente, que Candida albicans es una de las principales causas de mastitis o de dolor en los pezones. A muchas mujeres con sospecha de mastitis se les ha administrado antifúngicos por vía oral y/o tópica durante un tiempo prolongado sin mejoría, o incluso con un empeoramiento del cuadro clínico. Lo más sorprendente es que el diagnóstico de candidiasis «mamaria» se hace, en (casi) todos los casos, sobre la base exclusiva de la inspección visual del pecho; y en algunos se diagnostica observando un pecho/pezón dolorido pero con un aspecto externo normal.
La revisión bibliográfica de los casos de mastitis atribuidos a Candida spp. demuestra la falta de evidencias para llegar a tal diagnóstico. C. albicans es el agente causal de la candidiasis oral (muguet) en niños y de la candidiasis vaginal en mujeres. Sin embargo, y a diferencia de lo que sucede con los estafilococos y estreptococos, la glándula mamaria no es precisamente un ecosistema adecuado para su crecimiento.
De hecho, el aislamiento de levaduras en casos de mastitis es muy raro. En el laboratorio Departamento de Nutrición y Tecnología de los Alimentos de la Universidad Complutense de Madrid, en el que se hace un análisis microbiológico exhaustivo, únicamente han identificado 4 casos de mastitis por levaduras en cerca de 4.000 muestras analizadas, y todos se resolvieron sin ningún tipo de problemas mediante el tratamiento con fluconazol.
Quizás el mito de la candidiasis mamaria provenga del hecho de que en un pequeño porcentaje de casos (5-6%) coexisten una mastitis estafilocócica en la madre y una candidiasis oral en su hijo. Este hecho se debe a que los estafilococos, al crecer, producen una serie de compuestos que estimulan el crecimiento de las levaduras. Normalmente, los humanos solemos tener una pequeña concentración de levaduras en la cavidad oral desde nuestra más tierna infancia y de forma completamente asintomática. Sin embargo, durante una mastitis estafilocócica la concentración de estafilococos en la leche es muy superior a la normal, lo que puede estimular una excesiva proliferación de C. albicans.
Obviamente, un niño con muguet transfiere levaduras a la piel del pecho de la madre, lo que explica que en la leche de estas mujeres se pueda detectar una pequeña concentración de levaduras (<100 unidades formadoras de colonias [UFC]/mL). Ello no justifica que, ante una concentración de levaduras de 50 UFC/mL y una concentración superior a 500.000 estafilococos/mL, se llegue a un diagnóstico de… ¡candidiasis!.
Factores predisponentes
Tradicionalmente se han propuesto diversos factores que pueden favorecer el desarrollo de una mastitis infecciosa. Sin embargo, en la actualidad sabemos que hay dos que destacan por su importancia:
- la respuesta del sistema inmunitario del hospedador y su interacción con la cepa bacteriana que causa la infección, y
- la administración de antibióticos sin una base racional.
En el primer caso, conviene tener en cuenta que, para el sistema inmunitario, el control de las infecciones intramamarias resulta bastante más complicado que el de otro tipo de infecciones; por una parte, la leche tiene un efecto diluyente sobre los factores inmunitarios reclutados por el tejido mamario y, por otra, la grasa y las caseínas de este fluido biológico ejercen un efecto bloqueador sobre estos mismos factores. Para evitar tales efectos, el suministro de efectores inmunológicos a la glándula mamaria debe ser continuo y en una cantidad mucho más elevada que la necesaria para la protección de otros tejidos u órganos. Algunas de las bacterias causantes de mastitis pueden doblar su población cada 30-40 minutos, por lo que se requiere un reclutamiento muy rápido de neutrófilos sanguíneos y anticuerpos opsonizantes (especialmente de la subclase 2 de la IgG) durante las primeras 12-18 horas postinfección. En tales casos, el tráfico de neutrófilos circulantes hacia el tejido extravascular es tan rápido, que la vida media de estos leucocitos en la sangre es de sólo 4-10 horas. Lamentablemente, no siempre se puede mantener dicho ritmo y, de hecho, se ha observado una fuerte relación inversa entre la capacidad de reclutamiento de neutrófilos de la glándula mamaria y el desarrollo de una infección intramamaria. Por tanto, el correcto funcionamiento del sistema neutrófilos/anticuerpos opsonizantes es crítico para la prevención o la minimización de los síntomas locales y sistémicos de infección. La población de linfocitos y macrófagos residentes en la glándula mamaria desempeña un papel muy importante en el mantenimiento del citado sistema. En ocasiones, las cepas de Staphylococcus aureus implicados en estos casos pueden alterar completamente la respuesta inmunitaria normal mediante la producción de superantígenos. Además, algunas cepas bacterianas causantes de mastitis podrían tener otro mecanismo para eludir el sistema inmunitario: mimetizarse con el hospedador. Es decir, tendrían capacidad para «copiar» ciertas secuencias que forman parte de los antígenos del hospedador.
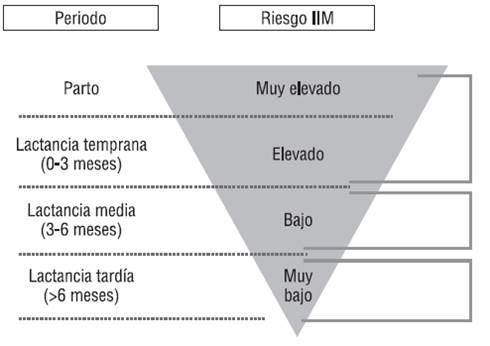
Figura: Riesgo de infección intramamaria (IIM) a lo largo de la lactancia en función de diferentes factores inmunitarios implicados (ver texto y bibliografía)
El segundo factor predisponente es el uso indiscriminado de antibióticos durante el último tercio del embarazo, el parto y/o la lactancia. La glándula mamaria se coloniza con bacterias (estafilococos, estreptococos, bacterias lácticas, bifidobacterias, etc.) procedentes del intestino materno durante el último tercio del embarazo. Entre ellas, un pequeño porcentaje de estafilococos poseen genes de resistencia a antibióticos, especialmente frente a betalactámicos. Al aplicar el antibiótico, se genera una disbiosis de la microbiota mamaria, de tal manera que desaparecen las bacterias sensibles pero se seleccionan las resistentes, que crecen sin competencia y alcanzan concentraciones muy superiores a las normales, lo que conduce a una mastitis infecciosa.
El número de cepas de S. aureus resistentes a meticilina aisladas de casos de mastitis ha aumentado espectacularmente en los últimos años. Paralelamente, se ha observado un notable aumento del porcentaje de mastitis asociadas a antibioterapia, que se suelen caracterizar por una presentación mucho más precoz que las mastitis infecciosas «tradicionales», y los primeros síntomas pueden aparecer incluso entre el primer y el séptimo día posparto. Posiblemente, una de las principales causas de este aumento es el uso inadecuado del protocolo para la prevención de las sepsis neonatales por estreptococos del grupo B (EGB). Los EGB constituyen una de las principales causas de morbilidad y mortalidad perinatal y, por ello, se toma una muestra de exudado vaginal entre las semanas 35 y 37 de gestación para su cultivo, con el fin de detectar la presencia de estas bacterias. En caso positivo, se administra un antibiótico (habitualmente penicilina G) por vía intravenosa durante el parto.
Este protocolo ha sido eficaz para reducir la tasa de sepsis, desde 1,8 hasta 0,4-0,6 casos por 1.000 neonatos. Sin embargo, la aplicación de esta profilaxis de forma indiscriminada debería ser objeto de una revisión crítica. Los EGB forman parte de la microbiota fisiológica del tracto intestinal y/o vaginal del 4-40% de las mujeres. A pesar de que la tasa de transmisión de madres a hijos puede ser de hasta un 75%, sólo el 1-2% de los niños nacidos de mujeres EGB-positivas (que no reciben profilaxis) desarrollan sepsis. La Academia Americana de Pediatría (AAP) y el Center of Disease Control USA (CDC) como el Documento de «Consenso Español para la Prevención de la infección perinatal por estreptococo del grupo B. Recomendaciones españolas revisadas 2012» recomiendan que el tratamiento antibiótico se administre tanto a mujeres EGB-positivas como a las que presenten determinados factores de riesgo.
Lamentablemente, estamos asistiendo a menudo a casos de mastitis por estafilococos resistentes a la penicilina G en mujeres que han recibido antibioterapia intraparto. Resulta paradójico que, mientras que las autoridades sanitarias nos están advirtiendo de los riesgos del abuso de antibióticos a través de la prensa y la televisión, estemos administrando antibióticos a un 20-25% de neonatos. Conviene considerar que el intestino del feto a término no es estéril y que ya contiene pequeñas concentraciones de estafilococos, estreptococos, bacterias lácticas y bifidobacterias, entre otras bacterias.
Por tanto, también se somete a estas bacterias a un proceso de selección entre las resistentes al antibiótico aplicado y a otros afines. En los últimos años ya se han anunciado los primeros efectos secundarios de la profilaxis: una mayor tasa de enfermedades alérgicas y una mayor dificultad para el tratamiento de infecciones. Por otra parte, resulta evidente que el tratamiento de mujeres EGB-positivas ha conducido a una notable reducción de la tasa de sepsis por estas bacterias, pero no a su desaparición. De hecho, se está observando un preocupante incremento en las poblaciones de EGB resistentes a la penicilina G en particular, y a los betalactámicos en general, debido a una mutación.
En conclusión, no se trata de desproteger a los niños que pueden estar en riesgo, sino de identificar los marcadores que eviten que la protección de un niño conlleve la aplicación sistemática de un protocolo que podría perjudicar innecesariamente a otros 999 y/o a sus madres. Por reducción al absurdo, se podría recomendar que ninguna mujer amamantara a su hijo como medida profiláctica frente a la sepsis neonatal ya que, aunque muy ocasionalmente, se ha observado que la leche humana puede servir de vehículo para cepas de EGB, S. aureus o Salmonella que han provocado sepsis neonatales. Obviamente, el daño que tal medida provocaría en la Salud Pública sería infinitamente mayor que el beneficio que proporciona. Desafortunadamente, el riesgo cero no existe.
En cualquier caso deberían administrarse probióticos clásicos o mejor de última generación (Lactobacillus salivarius o Lactobacillus fermentum) a todas las madres que recibieran tratamiento antibiótico por la razón que sea. (ver más adelante).
Diagnóstico de las mastitis: el cultivo de la leche.
Para diagnosticar una mastitis, saber que germen la causa y definir el tratamiento más adecuado debe realizarse siempre cultivo de la leche y no sólo en caso de mastitis aguda con sintomatología florida, también en caso de dolor (sugerente de mastitis subaguda) y/o escasa producción de leche (hipogalactia).
Habitualmente, el tratamiento de la mastitis se instaura de forma empírica y suele consistir en la prescripción de cloxacilina, amoxicilina, amoxicilina-ácido clavulánico, mupirocina o eritromicina. Pero un porcentaje cada vez más elevado de cepas implicadas en la mastitis son resistentes a estos antibióticos. Por este motivo, una parte de las mastitis tratadas con antibióticos derivan en una infección crónica o recurrente. Además, en los cultivos de leche es frecuente aislar dos o más especies implicadas en un mismo caso de mastitis y, si todas ellas no son sensibles al antibiótico elegido, se puede eliminar uno de los agentes causales pero fomentar el crecimiento de la bacteria resistente. En conclusión, el tratamiento de las mastitis infecciosas debería instaurarse tras un análisis microbiológico que determine el agente causal y su sensibilidad a los antibióticos.
Ante la ausencia de un diagnóstico etiológico y la frecuente prescripción de un tratamiento inadecuado, las mujeres con este problema suelen enfrentarse a un difícil dilema:
a) seguir amamantando a su hijo aguantando el dolor y el resto de síntomas lo mejor posible y, en muchos casos, ante la incomprensión de su propio entorno médico y/o familiar, o
b) abandonar la lactancia. Sin embargo, un número creciente de mujeres lactantes que se encuentran ante este problema exigen una tercera vía: un correcto diagnóstico y un tratamiento acorde con su caso particular.
La implantación sistematizada de los cultivos de leche en los servicios de microbiología de los hospitales puede ofrecer una solución para un buen porcentaje de casos.
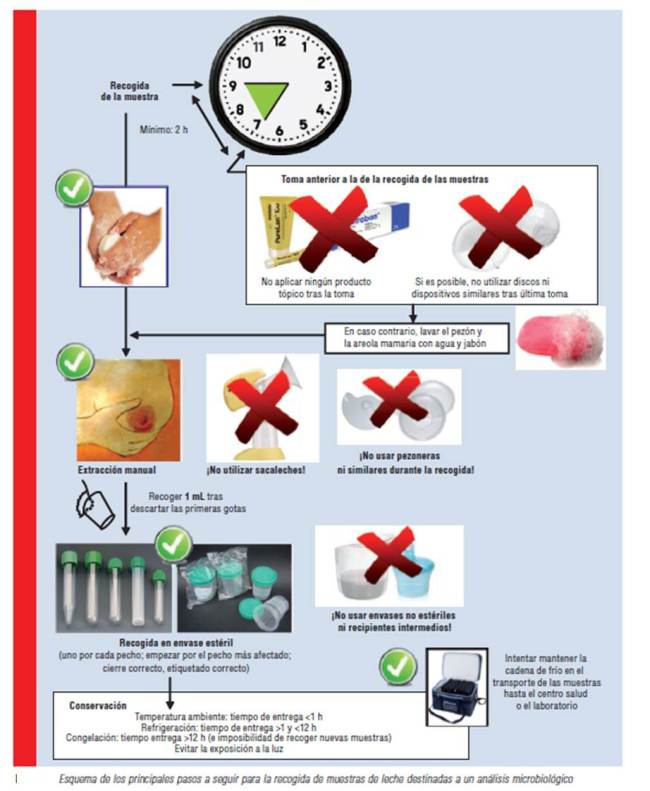
Obtención y conservación de las muestras (figura)
1. Las muestras se deben recoger inmediatamente antes de una toma y, si es posible, tras haber trascurrido al menos 2 horas desde la toma anterior.
2. Tras la toma anterior a aquella en la que se vayan a recoger las muestras para el cultivo, no se debe aplicar ningún tipo de pomada o solución tópica (lanolina, antibióticos, antisépticos, antiinflamatorios, productos de homeopatía…) ni tampoco utilizar ningún tipo de accesorio (conchas…) que provoque una acumulación de leche en contacto directo con las areolas mamarias y los pezones; en caso contrario, se deben lavar dichas partes del pecho con agua templada y jabón neutro, y secarlos con una toalla limpia o una toallita de un solo uso inmediatamente antes de la recogida.
3. Inmediatamente antes de la recogida, la paciente debe lavarse las manos con agua caliente y jabón (o un producto similar) y secárselas con una toalla limpia o una toallita de un solo uso.
4. Tras la estimulación previa del pecho, la recogida de muestras de leche destinadas a un análisis microbiológico se debe efectuar mediante presión manual, sin la ayuda de ningún tipo de accesorio (pezoneras, formadores de pezones…). En ningún caso se deben emplear extractores (sacaleches). Todos estos utensilios pueden ser una fuente importante de microorganismos ajenos a la glándula mamaria, que persisten tras la aplicación de los protocolos de limpieza y/o desifección recomendados por los fabricantes. Por tanto, su presencia puede enmascarar los verdaderos agentes responsables de una mastitis. En general, los microorganismos contaminantes suelen ser enterobacterias, Pseudomonas spp. y afines (Stenotrophomonas spp., etc.) y levaduras, que acostumbran a estar ausentes o presentes en concentraciones muy bajas en la leche humana. Muchos de ellos son psicrotrofos (resistentes al frío) por lo que siguen proliferando durante la conservación de la leche refrigerada. Por otra parte, conviene recordar que el agua potable con la que se lavan o aclaran las bombas y otros accesorios suele contener cantidades relativamente elevadas de algunos de estos microorganismos.
5. Las muestras de leche se deben recoger en envases estériles, como los empleados habitualmente para el análisis de muestras de orina o heces. Hay que recoger una muestra de cada pecho (cada una en un envase independiente), empezando por el pecho que esté menos afectado en el momento de la recogida, descartando las primeras gotas de leche (aunque este hecho parece no afectar significativamente al resultado del análisis microbiológico). Si los dos pechos tienen aproximadamente el mismo nivel de afectación, el orden es indiferente. El recipiente se debe colocar debajo del pezón, dentro de la areola mamaria.
6. Evitar tocar el interior del frasco o del tapón con los dedos, así como el contacto con cuerpos extraños.
7. No utilizar nunca recipientes intermediarios (cucharas, biberones, vasos, botellas, etc.) para recoger la leche antes de transferirla al envase estéril.
8. El volumen necesario para el cultivo de una muestra de leche es de 1 mL. Habitualmente, se siembra la muestra sin diluir y las diluciones –1 y –2 (5-50 μL por medio de cultivo).
9. Cerrar perfectamente el frasco para evitar derramamientos durante su transporte.
10. Rellenar una etiqueta con el nombre, apellidos, pecho del que procede la muestra y fecha y hora de la recogida. Pegar la etiqueta sobre el frasco seco. Obviamente, esto no será necesario cuando el análisis se realice en un centro de salud mediante el volante correspondiente ya que, en tal caso, llevará un código identificativo.
11. Las muestras pueden permanecer sin refrigerar un máximo de 1 hora. Si el tiempo de entrega va a ser superior a 1 hora, se pueden mantener en refrigeración a 4º C durante un máximo de 12 horas. Si el tiempo de entrega de las muestras va a ser superior a 12 horas, y no hay posibilidad de obtener nuevas muestras, es preferible conservarlas congeladas a una temperatura igual o inferior a –20 ºC, sin que se rompa la cadena de frío.
Siembra de las muestras
Los medios de cultivo más adecuados son el agar Columbia con ácido nalidíxico (CNA; aislamiento de estafilococos, estreptococos, enterococos, corinebacterias…), el agar Baird Parker (BP; aislamiento de estafilococos), el agar MacConkey (MCK; aislamiento de enterobacterias) y el agar Sabouraud dextrosa con cloranfenicol (SDC; aislamiento de levaduras). Entre todos ellos, el único medio imprescindible es el CNA (o, en su defecto, algún otro tipo de agar sangre), ya que permite el crecimiento simultáneo de la mayoría de las especies causantes de mastitis. Los medios MCK y SDC se emplean fundamentalmente para comprobar que no ha habido contaminación de las muestras. En principio, cualquier técnica de siembra de muestras biológicas es aplicable a las muestras de leche: desde la técnica de siembra con asa calibrada de 5 μL en forma de estría longitudinal, seguida de agotamiento total de la placa (muy extendida en los servicios de microbiología de los hospitales), hasta los sistemas semiautomáticos de siembra en espiral. Cualquiera de ellas permite la cuantificación de los microorganismos presentes en la muestra.
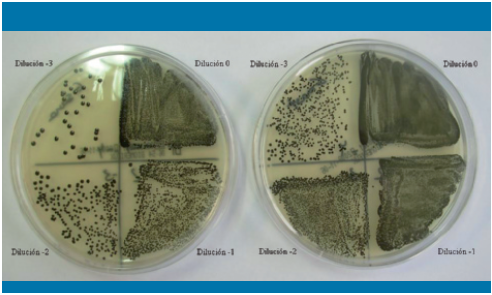
Placas de medio Baird Parker tras la siembra y la incubación de muestras de leche humana. Izquierda: mastitis por Staphylococcus aureus; derecha: mastitis por Staphylococcus epidermidis
Las placas sembradas se deben incubar a 35-37 ºC en atmósfera aerobia, con placa invertida. La lectura se debe realizar a las 24-48 horas. Los resultados recogerán la concentración de cada especie presente en la muestra, expresada en unidades formadoras de colonias (UFC) o simplemente «colonias»colonias (UFC)/mL. El hecho de no observar colonias en las placas no significa que no haya bacterias en la muestra, sino que éstas pueden estar presentes en una concentración inferior a la de su límite de detección. En tal caso, el resultado será «no se detecta crecimiento bacteriano» o «inferior al valor del límite de detección» (p. ej., 100 UFC/mL).
La identificación de las especies implicadas no debería plantear ningún problema para un laboratorio de microbiología clínica. Para ello, se pueden utilizar diversas técnicas (clásicas, Wider, Vitek, MALDI-TOF…). Posiblemente, el mayor reto estribe en una correcta identificación de algunas de las especies de estreptococos del grupo viridans, ya que son difíciles de diferenciar tanto en los medios de cultivo como con algunos de los procedimientos de identificación habituales.
Interpretación de los resultados
La mayor o menor severidad de la sintomatología asociada a una mastitis está estrechamente relacionada con la especie o las especies bacterianas implicadas, su concentración, las características de la cepa y el estado del hospedador.
Cuando se analizan muestras de leche resulta fundamental no considerar la presencia de estafilococos coagulasa-negativos (especialmente S. epidermidis) y estreptococos del grupo viridans (especialmente S. mitis y S. salivarius) como «flora contaminante» o «flora saprofita», sino como agentes potencialmente causantes de mastitis.
Desafortunadamente, esa apreciación suele ser habitual y conduce a un diagnóstico erróneo. En este sentido, la presencia de estas especies en leche siempre debe considerarse relevante, como sucede con S. epidermidis en muestras de infecciones hospitalarias asociadas a catéteres. Por consiguiente, se debe proceder a determinar su antibiograma.
En condiciones fisiológicas, la concentración de estafilococos coagulasa-negativos, estreptococos del grupo viridans y bacterias afines (Rothia spp., Kocuria spp., etc.) en muestras de leche recogida en las condiciones descritas anteriormente suele oscilar entre 100 y 300 UFC/mL, con un límite máximo de, aproximadamente, 1.000 UFC/mL. Cualquier valor por encima de esta concentración puede ser compatible con una mastitis infecciosa. No obstante, el valor suele estar notablemente aumentado (>5.000 UFC/mL).
S. aureus y Corynebacterium spp. no suelen estar presentes en la leche humana en condiciones fisiológicas y pueden provocar mastitis en concentraciones mucho más bajas que las especies antes citadas (<500 UFC/mL).
La presencia de bacterias gramnegativas (E. coli, otros coliformes, Stenotrophomonas…)
y levaduras suele estar asociada a un protocolo inadecuado de recogida de las muestras. En tales casos, pueden estar presentes en concentraciones elevadas para este tipo de muestras (>1.000 UFC/mL).
Tratamiento de las mastitis
Debe basarse en el cultivo, identificación y antibiograma.
La siguiente tabla relaciona cada tipo de mastitis con los agentes etiológicos, la sintomatología característica y el tratamiento empírico más adecuado. La propuesta de tratamiento está fundamentalmente dirigida a los casos en que no sea posible la realización de cultivos y antibiogramas y/o en los que no se pueda esperar a los resultados para iniciar el tratamiento.
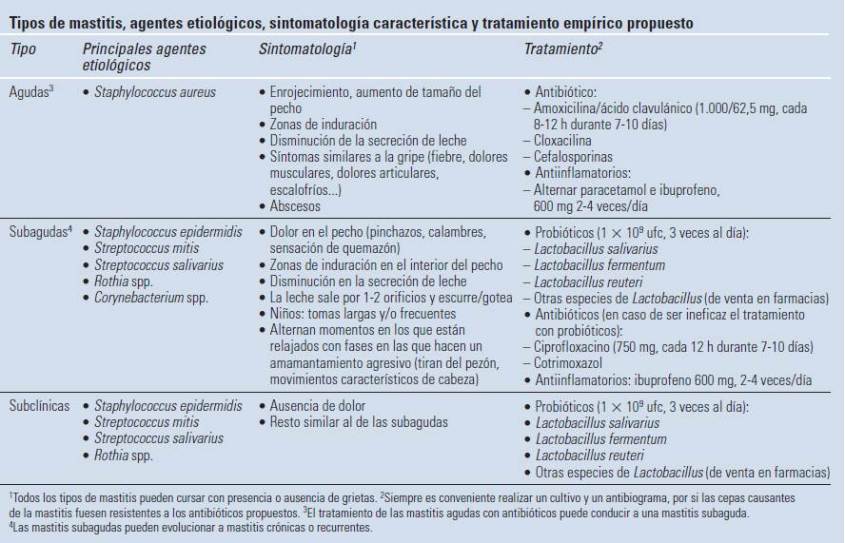
Tratamiento empírico de las mastitis agudas
Ante un cuadro agudo es razonable iniciar un tratamiento antibiótico. Se suele prescribir un betalactámico (cloxacilina o amoxicilina con/sin ácido clavulánico). La opción más recomendable, en ausencia de cultivo, sería amoxicilina+ ácido clavulánico (1.000/62,5 mg) en comprimidos de liberación prolongada. La cloxacilina tiene una eficacia es bastante limitada frente S. aureus (>50% de las cepas de S. aureus causantes de abscesos son resistentes a la meticilina). Son preferibles dosis altas que minimice la generación de cepas resistentes. La concentración de antibiótico en la leche no es directamente proporcional a la a la dosis administrada. (Ver www.e-lactancia.org para comprobar los riesgos de fármacos, fitoterapia (plantas), homeopatía y otros productos alternativos, procedimientos médicos y cosméticos, contaminantes, enfermedades maternas y del lactante y más).
El tratamiento con betalactámicos puede conducir a tres situaciones:
- Que el tratamiento sea eficaz y que el problema se solucione por completo, aunque, desafortunadamente, no es la situación más frecuente;
- Que las cepas de S. aureus implicadas sean resistentes, de tal manera que el cuadro no sólo no mejora, sino que se mantiene e incluso puede empeorar al crearse un ambiente propicio para el crecimiento selectivo de dichas cepas, y
- Que sea eficaz frente a S. aureus pero que seleccione el crecimiento de estafilococos coagulasanegativos o estreptococos.
Este último caso suele ser bastante común, de tal manera que la mastitis aguda se transforma en subaguda y, a partir de ese momento, habría que tratarla como tal.
Nivel de riesgo y parámetros cinéticos de diversos medicamentos empleados en el tratamiento de las mastitis

Tratamiento empírico de las mastitis subagudas y subclínicas
En general, los agentes causantes de mastitis subagudas y subclínicas son más resistentes a la antibioterapia pero, afortunadamente, responden bastante bien al tratamiento con probióticos. Los probióticos son microorganismos vivos que ejercen efectos beneficiosos sobre un hospedador y tienen diversas aplicaciones, reales o potenciales, en el binomio madre-hijo.
Recientemente, dos ensayos clínicos (Referencias 4 y 8 de la página de bibliografía) han demostrado que ciertos lactobacilos aislados de leche humana representan una alternativa más eficaz que los antibióticos para el tratamiento de las mastitis, y no presentan los efectos secundarios de éstos (candidiasis, trastornos digestivos…).
En general, algunas cepas de Lactobacillus salivarius aisladas de leche humana (CECT5713 o PS2) parecen ser las mejores candidatas para el tratamiento de las mastitis subagudas ya que son eficaces en más de un 90% de los casos. Los efectos probióticos dependen de cada cepa, las condiciones de empleo y su posología. En el caso de las cepas de L. salivarius citadas anteriormente, la dosis recomendable con fines terapéuticos sería de 109 ufc, 3 veces al día, durante 2-3 semanas, mientras que se podría tomar una dosis diaria de 109 ufc con fines preventivos. La cepa L. salivarius PS2 podría comercializarse en nuestro país en un futuro próximo para dicha indicación.
Ya está comercilizada otra cepa aislada de leche humana (L. fermentum CECT571613, eficaz en un 65-70% de los casos) con el mismo fin. Se denomina Lactanza Hereditum elaborado y comercializado por Angelini. Cuesta casi un € por cápsula. Todo sea por la lactancia materna. Seguir leyendo »


















